采用PBPK模型分析不同释放机制的盐酸文拉法辛缓释制剂生物等效性
推荐理由
缓释制剂的仿制药开发过程中,如果仿制药的缓释机理相比于原研有明显的不同,那么这种不同的释药机理极有可能引起两个制剂体内的生物不等效。采用生理药动学(PBPK)与吸收模型,能够对不同释放机制的两种制剂进行虚拟临床试验研究,并评估不同释放行为对体内等效性的影响,从而指导新制剂的开发并规避产品失败的风险。
原文献作者
Ho-Pi Lin, Dajun Sun,Xinyuan Zhang, Hong Wen
美国FDA,CDER,仿制药办公室OGD

导 读
盐酸文拉法辛Venlafaxine在临床上用于治疗抑郁症和其他精神疾病。本案例以盐酸文拉法辛作为模型药物,采用生理药代动力学PBPK模型,考察基于骨架控释的仿制制剂与基于渗透泵释放的参比制剂,其不同的释放行为对体内PK的影响;并基于验证后的PBPK模型,进一步评估了可打开的骨架缓释片的延迟释放时间(lag time)及不同释放行为其体内生物等效性的风险。
1. 研究背景
盐酸文拉法辛是一种5-羟色胺和去甲肾上腺素重吸收抑制剂,目前被开发成速释制剂和缓释制剂,临床上用于治疗抑郁症和其他精神疾病。
盐酸文拉法辛市场上有2个缓释的RLD产品,其中一个是基于扩散控释的包衣小丸胶囊(Effexor XR by Wyeth Pharmaceuticals Inc. [Pfizer],approved in 1997),另一个是渗透泵片(Venlafaxine HCl ER tablets by Osmotica Pharmaceutical Corporation, approved in 2008)。
2005年,印度太阳制药拟开发基于可打开的骨架型控释机理的文拉法辛缓释片,参比制剂的选择上向FDA递交了以Effexor XR Capsules作为RLD制剂的请愿,并获允许。美国Osmotica公司在2008年通过申请,要求目前尚未获批的ANDAs申请应以该公司的venlafaxine HCl ER tablets 作为指定的RLD制剂。印度太阳制药后续又不得不经生物等效性试验证明与Osmotica公司的产品等效后,其仿制药在2010年最终获FDA批准。
机制性的吸收模型和PBPK模型已被证明是评估药物体内行为和生物等效性的有力工具,并已应用于仿制药上市后监测和生物等效性评价。本案例中采用文拉法辛作为模型药物,采用GastroPlus软件考察两种不同释放机制的缓释片剂其不同释放行为对体内PK的影响,并进一步评估两种制剂体内生物等效性的风险。
两种缓释制剂的释放机理如下:
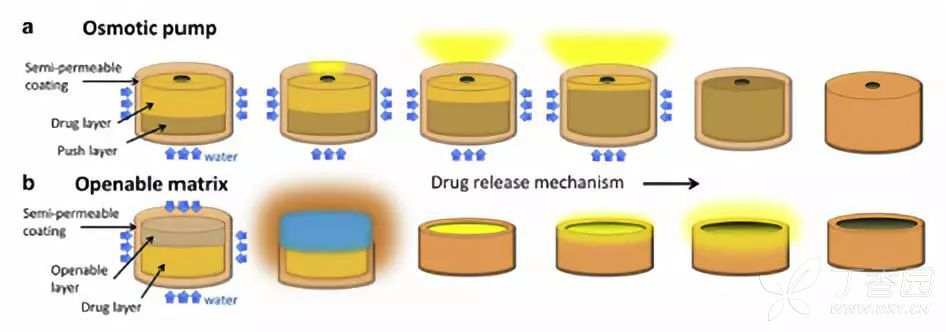
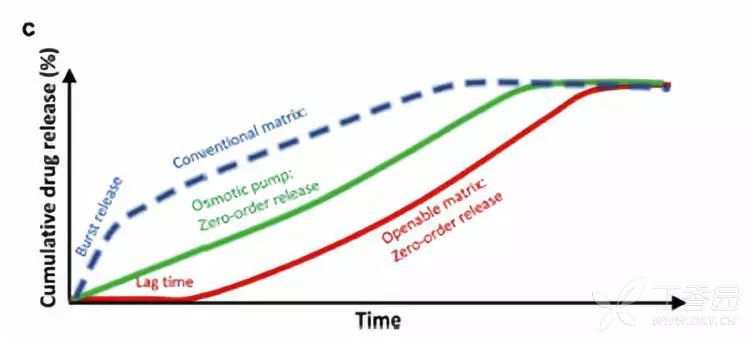
其中,a为渗透泵缓释片,水由半透膜包衣渗入片芯,使推动层吸水膨胀,促进药物释放;b为可打开骨架缓释片,外层包含一层功能性包衣,水渗入片芯,可打开层吸水溶胀使包衣层破裂,含药层与溶出介质接触进而释放药物;c为3种释放机理的缓释制剂不同的释放行为,其中传统骨架片前期存在突释现象,渗透泵片按照零级速率进行释放,可打开的骨架片前期存在明显的释放延迟,后期同样按照零级速率进行释放。可打开骨架片与渗透泵片相比,前期的释放延迟是有可能造成两种制剂体内生物不等效的关键风险因素。
2 . 建模数据与处理
2.1 盐酸文拉法辛的相关建模参数
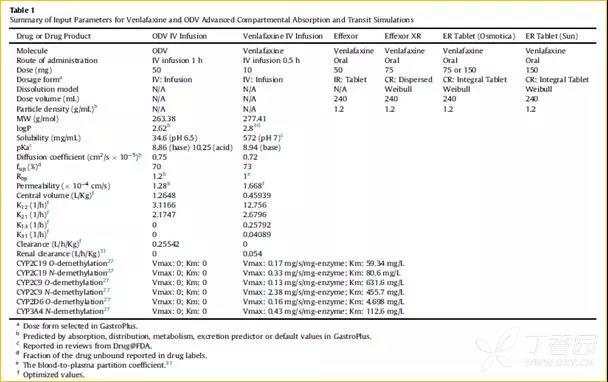
溶解性:
文拉法辛为BCSⅠ类药物,易溶于水,水中的溶解度为534mg/mL,其主要的代谢产物ODV同样易溶于水;
有效渗透性Peff:
文拉法辛在人体肠道内的有效渗透性是通过盐酸文拉法辛速释片的体内PK数据进行拟合的;
代谢与清除:
文拉法辛体内被CYP450酶广泛代谢,包括CYP 2D6,2C9和2C19,其中2D6是最主要的代谢酶;因此模型中文拉法辛的清除途径被设置为肠道和肝脏的代谢清除,清除率通过各代谢酶的Vmax和Km值转化,其中Km值为体外肝微粒体试验数值,Vmax为模型优化的数值。
体内PK数据:
盐酸文拉法辛缓释胶囊和渗透泵片75mg规格的临床PK数据来源于NDA的综述资料中;文拉法辛静脉注射、盐酸文拉法辛渗透泵片和可打开骨架片的完整PK数据未能从公开资料中获取。
其他输入参数,如logP、pKa、Fup(%)、Rbp等为软件预测值或来源于申报资料中。
3 . 模型结果与分析
3.1 口服单剂量盐酸文拉法辛IR(速释)和ER(缓释)制剂后的PK曲线预测结果
本案例中,采用GastroPlus软件中的PKPlus模块,分别拟合文拉法辛和其代谢产物ODV的IV数据,分析文拉法辛的PK数据其最佳模型为3房室模型,ODV的PK数据其最佳模型为2房室模型。
下图中,红色代表文拉法辛,蓝色代表代谢物ODV;实线代表预测结果,点代表实测结果。其中文拉法辛静脉注射10mg,以及口服150mg渗透泵片和可打开骨架片的临床实测PK数据未能从公开资料中获取,因此预测结果的准确性通过比较Cmax和AUCt进行评估。
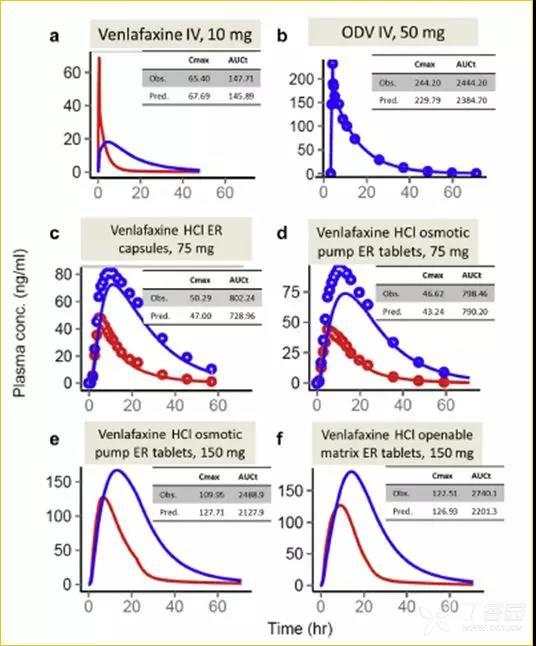
Figure 3 文拉法辛及代谢物ODV的PK模拟结果
图中原型药文拉法辛PK参数(如Cmax和AUCt)所有预测的结果均在临床实测的Cmax和AUCt平均值的20%变异范围内。且文拉法辛PK曲线的预测结果与实测结果整体趋势基本一致,如上图b-d所示。代谢物ODV的PK参数(如分布体积、清除率、K12、K21)是基于ODV静脉注射后的数据估算的,其他人群中的模拟均采用了该组数值;由于在特定人群中代谢物ODV的代谢和消除过程并不适用于其他人群,因此上图中ER制剂的ODV的预测结果相比于实测结果出现偏低的现象。此外,盐酸文拉法辛ER制剂生物等效性的评价标准是基于原型药的,所以ODV预测结果偏低的情况并不影响目前的生物等效性评价。
3.2 评估体外溶出行为对体内生物等效性的影响
ER制剂PK曲线的预测是通过Weibull方程,模拟体外不同条件下的溶出曲线然后预测体内PK,通过比较预测的PK曲线与临床实测PK曲线的拟合程度,来分析最佳的体外溶出条件,即与体内有相关性的溶出。
下图中曲线1-3为参比制剂渗透泵片体外溶出曲线,4-8为仿制药可打开骨架片体外溶出曲线;可打开骨架片在体外不同溶出条件下表现出了明显的溶出差异,而渗透泵片在不同条件下的溶出行为基本一致。
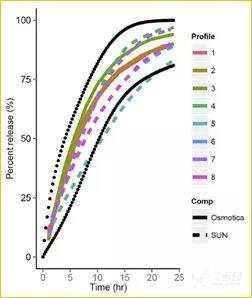

文拉法辛骨架缓释片模拟结果显示溶出方法4,即采用2-stage dissolution方法预测的结果与实测结果最为一致,因此溶出方法4作为代表骨架缓释片释放行为的标准溶出条件,进一步分析不同释放行为对体内生物等效性的影响;上图中黑色的两条释放曲线分别代表能够与方法4溶出代表的可打开骨架片体内生物等效的溶出上限和下限(按照80%的Cmax和125%的Cmax计算)。
预测结果见下表。
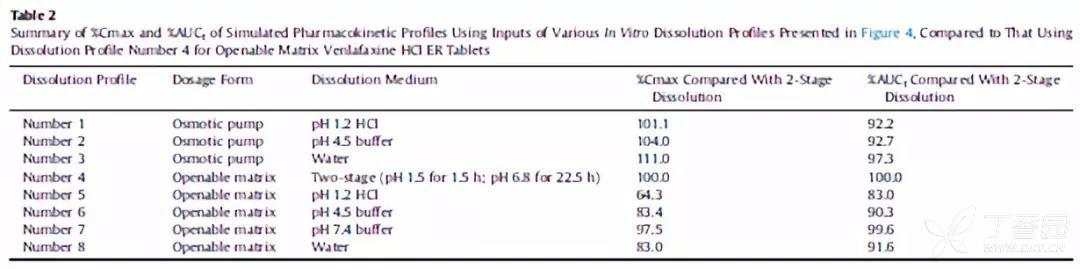
由模拟结果可知,除ph1.2外,其余各条件下的溶出预测体内PK结果,均在生物等效可接受范围内(ph1.2条件的溶出预测结果偏低,但考虑药片暴露在整个胃肠道如此低的ph并不现实,因此不需过分担忧该条件的影响)。因此,可打开骨架缓释片体外释放差异引起体内生物不等效的风险很小。
3.3 评估lag time对生物等效性的影响
可打开骨架片相比于渗透泵片,释放前期存在明显的释放延迟的现象。因此,为评估释放延迟时间对体内生物等效性风险的影响,模型中通过Weibull方程,设置lag time为0-4h的不同释放行为的曲线(图5),并预测相应的体内PK曲线(图6)。其中当lag time为0时,即代表参比制剂渗透泵片的释放行为,该曲线预测结果作为评估生物等效性的标准结果;其他lag time则代表仿制药可打开骨架片的不同释放行为。
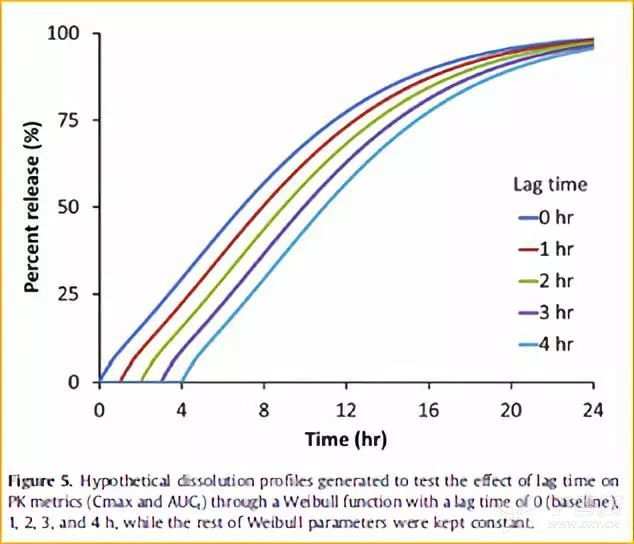
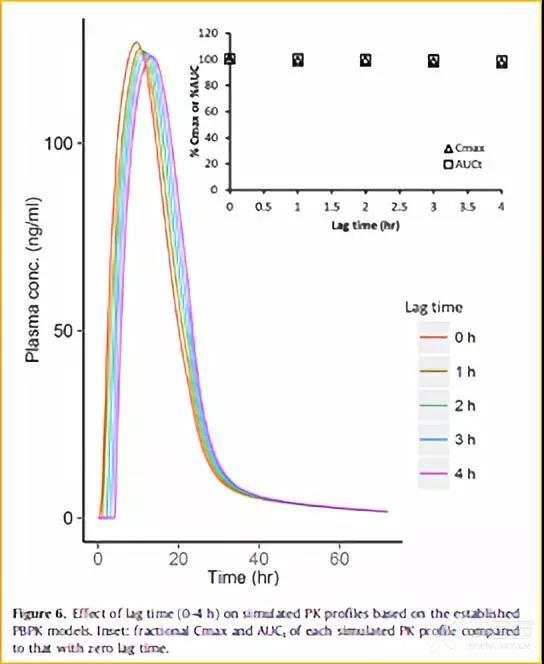
由模拟结果可知,lag time越大,即骨架片可打开层吸水溶胀使包衣层破裂的时间越长,则预测的Cmax和AUCt越小。但是当lag time为4h时,预测的PK结果(Cmax和AUCt)依然在生物等效可接受范围80%-125%内,说明可打开骨架片释放延迟时间并不是影响文拉法辛缓释制剂体内生物等效性的关键因素。
4 . 模型讨论
建立的PBPK模型中,选择合适的体外溶出数据作为模型中溶出输入参数来预测药物的体内释放至关重要。
对于渗透泵缓释片,体外溶出条件(如不同pH介质)对药物的释放行为无明显的影响,导致不同条件下的溶出曲线相似,因此基于体外溶出能够合理的预测体内的PK(图3d和3e);
对于可打开骨架缓释片,选择体内相关的体外溶出条件相对会比较复杂一些,因为骨架片中药物的释放会受多个因素影响,比如胃肠道中不同的pH以及不同部位的滞留时间等,如图4中,骨架片的释放速率随介质pH升高而增加。基于以上考虑本案例中最终选择了一个两个阶段的溶出条件(pH 1.5介质,然后转pH6.8介质),该条件认为最具有体内相关性,能够较好的预测可打开骨架片体内的PK曲线。
5 . 总结
该案例采用GastroPlus软件建立了盐酸文拉法辛ER制剂的PBPK吸收模型,并以2阶段溶出方法的体外溶出数据作为输入参数,准确预测了单剂量口服盐酸文拉法辛可打开骨架缓释片后的体内PK。建立后的模型进一步用于评估盐酸文拉法辛可打开骨架片潜在的延迟释放时间对体内生物等效性的影响。基于模拟的结果,即便延迟释放时间达到4h,虽然Tmax会稍有延迟,但预测的PK指标(Cmax和AUCt)仍满足生物等效的要求。
因此,基于PBPK模型的建模与模拟进行虚拟的临床试验研究,可以作为仿制药开发过程中,用于评估与产品释放、体内PK,以及生物等效性相关的关键质量属性的有效的工具手段。
6 . 应用软件与模块
该案例应用的软件是GastroPlus (version 8.6),涉及模块有Base, PBPK, Metabolism & Transporter, Optimization, ADMET Predictor。
7 . 参考文献
Ho-Pi Lin, et al. Physiologically Based Pharmacokinetic Modeling for Substitutability Analysis of Venlafaxine Hydrochloride Extended-Release Formulations Using Different Release Mechanisms: Osmotic Pump Versus Openable Matrix. Journal of Pharmaceutical Sciences 105 (2016) 3088-3096. IF: 2.713


