
什么是制剂体外崩解与溶出模拟软件DDDPlusTM ?
DDDPlus (Dose Disintegrationand Dissolution Plus)是由美国Simulations Plus公司开发的体外崩解与溶出模拟软件,用于模拟API及其制剂(速释制剂、缓释制剂、控释制剂以及长效注射制剂等)在体外不同溶出条件下的溶出或释放行为,以评估不同制剂处方、溶出条件等对体外溶出行为的影响,帮助用户筛选制剂处方、开发溶出条件、提高药品研发效率。
DDDPlus将溶出过程中涉及的一系列因素整合到模型公式中,如考虑原辅料的组成与相互作用、API粒度分布、溶出介质表层及内部的pH、溶出方法、机器转速等多种条件对溶出过程的影响,进而合理准确地模拟API及制剂的溶出曲线。
典型用户
FDA、中检院化药所、赛诺菲、GSK、台湾中环集团、国家纳米中心、军科院
浙江药检院、江苏药检院、湖北药检院、山东药检院、四川药检院
北京药检所、广东药检所、上海药检所、厦门药检院、内蒙古药检院
购买理由
可靠的产品性能:FDA, CFDA等法规部门信赖的体外溶出软件
独特的产品性能:内建多种剂型、溶出方法及溶出介质等
节省成本的利器:辅助处方设计、优化、筛选
完善的售后服务:专业应用支持,定期软件培训,用心技术交流
DDDPlusTM 主要用途
预测制剂的溶出曲线,指导制剂处方优化:预测处方辅料种类及用量、原辅料粒径及粒度分布、制剂工艺、剂型等多种条件改变后API及制剂的溶出曲线,从而辅助处方设计与优化
辅助体外溶出条件的筛选:软件可选择不同的溶出方法、仪器转速、介质体积、介质类型等,以全面筛选溶出条件 参数敏感性分析:使用者可寻找影响制剂溶出的敏感参数,如溶解度、粒径等,然后又针对性地改善制剂性质,优化溶出行为,提高药品质量 虚拟试验:可模拟一系列不同的溶出试验,考察制剂参数及溶出条件的差异性对溶出曲线的影响,指导制剂的生产,帮助科研人员建立更加合理的溶出标准
请回到该产品介绍顶部,查看模块简介、应用案例、资料文献、专题培训
DDDPlusTM 具体应用
虚拟试验(Virtual Trial)
模拟一系列不同的溶出试验,考察制剂参数及溶出条件的差异性对溶出曲线的影响,指导制剂的生产,帮助科研人员建立更加合理的溶出标准。
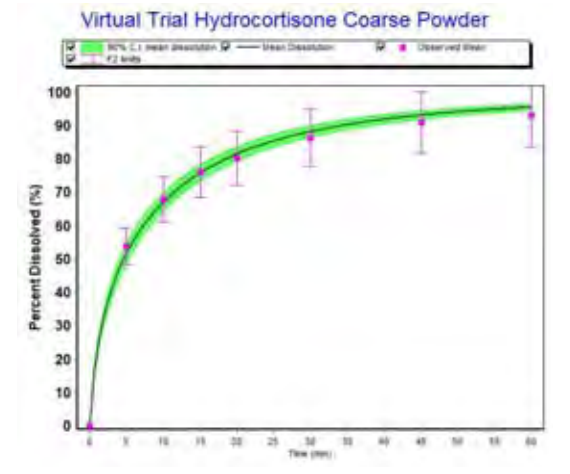
考察API用量及粒径的变异对其溶出曲线的影响并给出相似性的空间范围(f2因子判断)
制剂溶出条件的建立
内建90多种溶出介质(包拈USP、JP标准的溶出介质以及FaSSIF,FeSSlF等)
可选择不同种类及用量的表面活性剂、或者其它组成的缓冲盐以构建新的溶出介质
八种溶出方法/模型(转篮法、浆法、流通池法、微量溶出、转盘法等)
可设置不同的释放阶段, 模拟胃肠道不同pH环境, 辅助缓控释制剂的开发, 以及建立符合生理环境的体外溶出条件
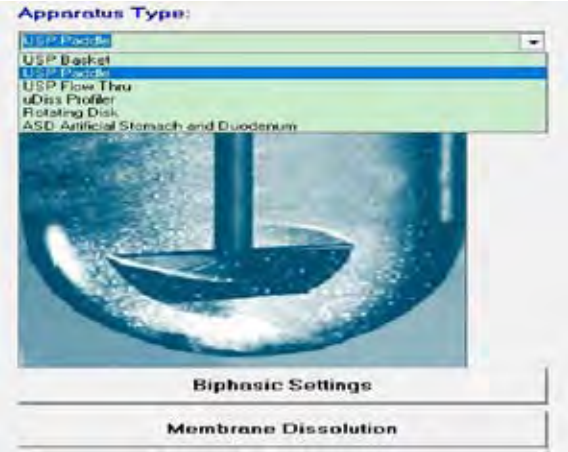
溶出条件选择界面:可选择溶出介质的种类、体积、pH、密度,溶出方法及机器转速等
参数敏感性分析 PSA(Parameter Sensitivity Analysis )
通过PSA,可寻找影响制剂溶出的敏感参数,如溶解度、粒径等,从而有针对性地改善制剂性质,优化溶出曲线,提高药品质量
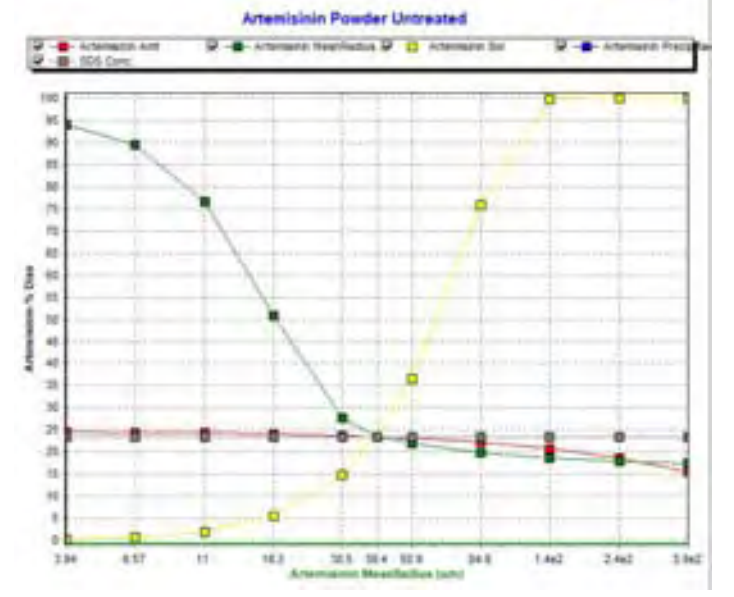
通过PSA可考察各个因素对溶出度的影响,更快速地寻找敏感性参数,以指导后续试验的进行
预测溶出曲线,优化制剂处方
预测制剂处方(辅料类型、原辅料用量等)、API粒径及粒度分布等多种条件改变后API及制剂的溶出曲线;
还可与参比制剂的溶出曲线进行相似性或差异性判断(f1、f2因子),以筛选出合适的制剂处方。
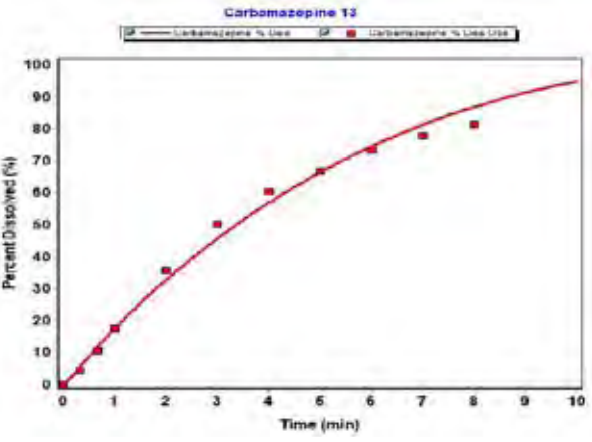
DDDPlus独特功能
内建40多种常用辅料
淀粉、乳糖、PVP、HPMC等的数据库,理化等性质参数一目了然,用户可选择不同的辅料,快速搭建出一种制剂处方。
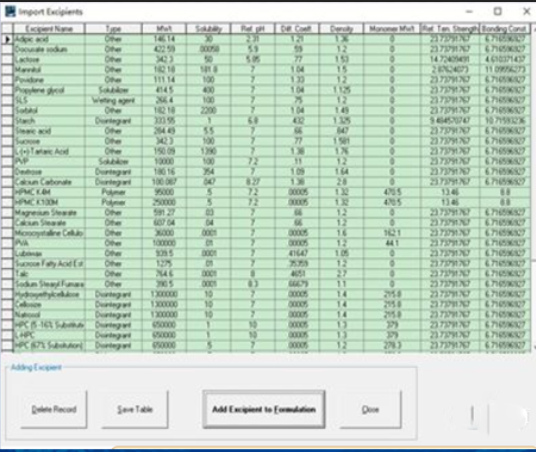
内建90多种溶出介质
USP、JP标准的溶出介质以及模拟空腹、饱腹状态的胃肠道生理介质,每种介质均可点开查看具体的组成;
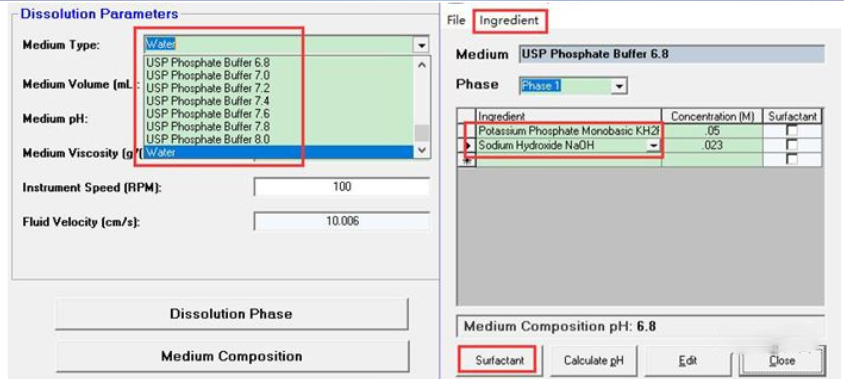
内建的溶出介质库
涵盖多种制剂剂型
软件内建了多种速释制剂(粉末、片剂、胶囊、溶液、包衣小丸等);缓控释制剂(可溶胀型或不可溶胀型骨架片、双层片、包衣小丸、肠溶包衣片等)以及长效注射制剂(注射用微球等)。

剂型的选择界面
内建标准的USP转篮法、浆法和流通池等溶出方法;
提供研发过程常用的微量溶出法和转盘法;
新增人工胃与十二指肠模拟液溶出、双相溶出及膜渗透等较新颖的溶出模型。
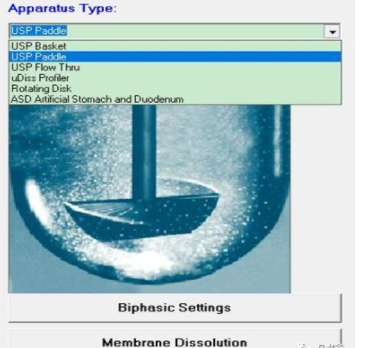
请回到该产品介绍顶部,查看产品概述、应用案例、资料文献、专题培训
【案例揭秘】 使用DDDplus软件模拟体外溶出行为
来源:【研如玉公众号】
摘 要 :溶出度测试是许多剂型(包括片剂和胶囊)的性能测试。
本研究的目的是评估计算机模拟是否可以预测两种模型药物的体外溶出度,而这两种不同药物的溶出数据可以获得。使用公布的孟鲁司特钠和格列本脲溶出数据用于模拟。评估了不同的药典和生物溶出度检测介质,体积和转速。另外,使用这些缓冲液评估一个pH值变化方案。DDDPlus™3,Beta版(Simulation Plus,Inc。)用于模拟体外溶出数据。将模拟数据与体外数据进行比较。使用预测数据和观察数据之间的回归系数来评估模拟。孟鲁司特钠统计分析显示,除一种缓冲液外,所有案例的体外释放数据与预测数据之间存在显著相关性。使用单一pH条件,格列本脲在实验数据与预测数据之间存在显著相关性。使用动态pH方案,对于一种生物溶出度介质是显著相关性。模拟显示体外药物释放都对溶解度效应敏感,这证实了它们的BCS归属 II类。使用DDDPlusTM的体外释放的计算机模拟具有在药物开发过程的早期阶段估计体内溶出的潜力。这可能用于选择最合适的溶出条件,以建立IVIVC并开发生物溶出度相关的体外性能测试,以通过设计空间捕获质量控制过程中的关键产品属性。
结 论
DDDPlus™能够预测不同实验条件下孟鲁司特钠和格列本脲的体外释放类型。使用DDDPlus TM的体外释放类型的计算机模拟具有在药物开发过程的早期阶段估计体外溶出行为的潜力。这可以用于选择最合适的溶出条件,一方面建立IVIVC,另一方面开发生物相关的体外性能测试,捕获质量源于设计方法中的关键产品属性或适当的质量控制程序。
阅读文章全部内容
请点击链接:https://mp.weixin.qq.com/s/lRXoboHrvjeYfnCV0sbQ7A
【大力推荐】使用体外和计算机模拟模型进行超出FDA现行标准的崩解试验的依据
来源:【研如玉公众号】
摘 要
药品性能测试是质量源于设计(QbD)方法的重要组成部分,但这个过程往往缺乏对所涉及崩解和溶解过程之间复杂相互作用的潜在机制的理解。尽管美国食品和药品管理局(FDA)最近的一份草案指南允许使用崩解试验替代溶出试验,但是这一标准并未在全球范围内被接受。本研究为使用崩解试验替代溶出试验作为某些速释制剂(IR)的质量控制方法提供了科学依据。提出了一种超出FDA现行标准的机械方法。使用USP浆法在不同的转速下对甲硝唑的速释和缓释制剂进行溶出试验。通过DDSolver进行溶出曲线拟合并通过DDDPlus进行溶出曲线预测。结果表明,Fickian扩散和药物颗粒属性(DPP)可用于解释IR片剂的溶出行为,并且这些制剂因素(例如圆锥形)仅在较低旋转速度下影响溶出行为。对于缓释片剂,DPP不重要时,溶出行为完全受处方控制。为证明当溶出度受DPP控制时,崩解是最重要的制剂属性,在常规和崩解影响介质(DIM)中进行崩解、固有溶出度和溶出测试。片剂崩解受到DIM的影响,并且符合Korsmeyer-Peppas方程的模型,其结果显示制剂在DIM中的溶出有所改善。DDDPlus能够预测片剂溶解在常规介质和DIM中的固有溶出曲线。该研究表明,崩解发生在DPP依赖的溶解之前。该研究表明,在FDA标准之外,崩解也可用作快速崩解片剂的性能测试。科学标准和理由是溶出必须是DPP依赖性的,源于API特征和制剂因素必须可忽略不计。
结 论
在药物开发过程中QbD方法的目标是充分描述和控制所有关键过程和质量属性。如今,基于对产品和工艺性能的全面了解,统计方法和计算机模拟可用于实现合理的产品设计并评估可能的工艺或产品风险。
本研究显示了DDDPlus目前在不同介质和转速下预测API和片剂溶出行为的能力和局限性。通过DDSolver的溶出模型拟合结果能够区分DPP和处方影响的片剂溶出行为。
该研究系统的研究了IR片剂的崩解和溶出行为。发现崩解和溶解可以是依次进行或同时进行的,或者依次进行或同时进行同时发生。如果首先发生崩解,则可能产生DPP主导的溶出过程,并且崩解可以用作速崩片的性能测试(超出FDA现行标准),其科学数据是,溶解与API的特性息息相关,同时依赖于DPP,溶出过程中的处方因素必须可以忽略不计。但是,如果处方显着影响溶出行为,则应将溶出用作质量控制方法。
这种方法将使全球运营的制药公司能够通过崩解试验科学地保证其产品质量规格,而不必非要去迎合可能互相矛盾的各国单独定制的监管指导文件。
阅读文章全部内容
请点击链接:https://mp.weixin.qq.com/s/AlTwCRkqIUIFSLwME9o7mw
【案例揭秘】 使用silico模拟溶出曲线开发多沙唑嗪缓释片
来源:【研如玉公众号】
摘 要
对制剂人员来讲,开发具有适当适当释放特性的缓释(ER)制剂有一定的难度。本研究的目的是通过使用计算模拟技术绘制具有统计学意义的释放曲线来实验设计多沙唑嗪缓释片的开发。试验制备多沙唑嗪缓释片,释放曲线测试条件:USP装置2;900ml不含酶的模拟胃液为介质;37±0.5℃和75rpm测试960min。试验结果填入模拟软件DDDPlus以优化校准常数。通过Design Expert软件调节乳糖和HPMC K100M的处方比例,制备7个不同的处方,使用DDDPlus模拟释放曲线。经过统计分析后,确认一个优化的多沙唑嗪缓释片处方,制备、检测,并与预测的曲线进行比较。两曲线的相关系数是0.99。使用模拟测试可以减少66.67%的分析工作时间,同时减少77.78%的仪器使用时间和介质体积。使用计算机模拟进行缓释制剂开发的实验设计,可以事半功倍。
结 论
使用DDDPlus和实验设计相结合的释放模拟可成功应用于多沙唑嗪缓释片剂的药物开发。并且,DDDPlus模拟可以通过减少需进行的实验数量来帮助公司节省时间和降低实验室成本。此外,处方设计的预测模型可用来对药物释放模型进行适宜的设计空间设置。
阅读文章全部内容
请点击链接:https://mp.weixin.qq.com/s/8YxjOuFoaPS-C0ylAQUeFA
【案例揭秘】高溶解和低溶解药物(按BCS分类)的固有溶出模拟
来源:【研如玉公众号】
摘 要
固有溶出测试是对药物以特有的表面积在特定溶出介质中的溶解速率进行表征。这可用于确定药物是高溶解度还是低溶解度。本文中,使用DDDPlus 4.0版(Simulations Plus,Inc。)进行乙胺嘧啶和甲硝唑的固有溶出实验。乙胺嘧啶低溶解度,甲硝唑高溶解度。软件预测的固有溶出速率(IDR)与体外实测的固有溶出速率比较。将每个药物的物化参数(文献值)和固有溶出速率测试的试验条件作为软件的输入数据。该程序能够预测乙胺嘧啶和甲硝唑在pH值1.0~7.2的IDR。两种药物的实测IDR和软件预测的IDR显示出高相关性(R2>0.9424)。模拟的IDR值显示乙胺嘧啶和甲硝唑在不同pH值介质中的溶解度,便于我们按BCS对其溶解度进行分类。使用DDDPlus进行固有溶出度模拟测试可用于获得某一药物的BCS溶解度分类,有助于减少实验室实验的数量。
讨 论
使用DDDPlus进行的计算机模拟可以帮助您在药物开发过程中获得对API的生物性能理解。可以使用软件模拟来预测API在生理相关pH值(pH1~7.2)的固有溶出。这可以帮助简化和最大程度地减少实验室实验工作。关键实验可以通过模拟识别,并通过实验结果加以确认,以表征API重要的生物性能。
阅读文章全部内容
请点击链接:https://mp.weixin.qq.com/s/uXZvgHKpMFNkZwt_yz9myg
请回到该产品介绍顶部,查看产品概述、模块简介、资料文献、专题培训
导 读
凡默谷技术部选取和汇总了2015-2020年制剂体外崩解与溶出模拟软件DDDPlus发表的应用文章,并将标题翻译成中文。
希望对您的业务或专业学习有所帮助,内容如下:
1. 采用基于生理的吸收模型,探讨食物和胃液pH值变化对恩曲替尼Entrectinib药代动力学的影响
Parrott N, Stillhart C, Lindenberg M, Wagner B, Kowalski K, Guerini E, Djebli N, Meneses-Lorente G. AAPS J (2020) 22:78. IF= 3.737
2. 使用基于生理的生物药剂学模型(PBBM)预测速释制剂空腹和餐后的生物等效性
Jereb R, Kristl A, Mitra A. Eur J Pharm Sci. Volume 155, 1 December 2020, 105554. IF= 3.616
3. 制剂处方开发早期的无定型固体分散剂:使用DDDPlus预测辅料对溶出曲线的影响
Njoku JO, Mukherjee D, Webster GK, Löbenberg R. Dissolut Technol.MAY 2020. IF= 0.674
4. 药物制剂早期开发的计算机预测工具:所需的数据和软件的功能
In silico Tools at Early Stage of Pharmaceutical Development: Data Needs and Software Capabilities.
Njoku JO, Amaral Silva D, Mukherjee D, Webster GK, Löbenberg R.AAPS PharmSciTech. (2019) 20: 243. IF=2.401
5. 采用生理药代动力学PBPK模型,评估影响美托洛尔缓释药品生物等效性的制剂因素
Sumit Basu, Haitao Yang, Lanyan Fang, Mario Gonzalez‐Sales, Liang Zhao, Mirjam N. Trame, Lawrence Lesko, Stephan Schmid. J Clin Pharmacol. Volume59, Issue9. September 2019 Pages 1252-1263. IF=2.425
6. 评估制剂处方变异对临床的影响:以美托洛尔缓释制剂作为研究案例
Evaluating the Clinical Impact of Formulation Variability: A Metoprolol Extended‐Release Case Study.
Kim S, Sharma VD, Lingineni K, Farhan N, Fang L, Zhao L, Brown J, Cristofoletti R, Vozmediano V, Ait-Oudhia S, Lesko LJ, Trame MN, Schmidt S. J Clin Pharmacol. May 14, 2019. IF=2.425
7. 建立体外-体内相关的溶出和转化建模策略-某研讨会总结汇总
Heimbach T, Suarez-Sharp S, Kakhi M, Holmstock N, Olivares-Morales A, Pepin X, Sjögren E, Tsakalozou E, Seo P, Li M, Zhang X, Lin HP, Mitra A, Morris D, Patel N, Kesisoglou F. AAPS J. Feb 11, 2019.IF=3.737
8. 用于体外-体内外推转化IVIVE的生理药代动力学PBPK建模:强调溶出数据的使用
Vivek M. Ghate, Pinal Chaudhari, and Shaila A. Lewis. Dissolut Technol. August 2019. IF= 0.674
9. 药品开发中的溶出测试:研讨会总结报告
Dissolution Testing in Drug Product Development: Workshop Summary Report
Andreas Abend, David Curran, Jesse Kuiper, Xujin Lu, Hanlin Li, Andre Hermans, Pramod Kotwal, Dorys A Diaz, Michael J Cohen, Limin Zhang, Erika Stippler, German Drazer, Yiqing Lin, Kimberly Raines, Lawrence Yu, Carrie A Coutant, Haiyan Grady, Johannes Krämer, Sarah Pope-Miksinski, Sandra Suarez-Sharp. AAPS J. 2019 Jan 28;21(2):21. IF=3.737
10. 通过计算机模拟溶出曲线,开发多沙唑嗪缓释片
In Silico Simulation of Dissolution Profiles for Development of Extended-Release Doxazosin Tablets.
Duque MD, Issa MG, Silva DA, Barbosa EJ, Löbenberg R, Ferraz HG.Dissolut Technol. NOVEMBER 2018. IF= 0.674
11. 用于评估膳食对缓释制剂释放的影响的生理学考虑和体外策略
Koziolek M, Kostewicz ES, Vertzoni M. AAPS PharmSciTech. Aug 28, 2018. IF=2.401
12. 采用体外方法评估空腹状态下,药物在小肠中的沉淀-PEARRL综述
In vitro methods to assess drug precipitation in the fasted small intestine – a PEARRL review.
O’Dwyer PJ, Litou C, Box KJ, Dressman JB, Kostewicz ES, Kuentz M, Reppas C. J Pharm Pharmacol. 2018 Jun 28. IF=2.571
13. 溶出过程中,十二烷基硫酸钠载药不完全和分散颗粒剂的扩散层内的空腹状态下的模拟肠液胶束
Kendra Galipeau, Michael Socki, Adam Socia, Paul A. Harmon.Journal of Pharmaceutical Sciences. 107 (2018) 156-169. IF=2.997
14. 针对BCS溶解度分类的高溶解度和难溶性药物的固有溶出度模拟
Duque MD, Issa MG, Silva DA, Kakuda BAS, Rodrigues LNC, Löbenberg R, Ferraz HG. Dissolution Technologies. 2017 Nov.IF=0.674
15. 使用体外和计算机模拟模型证明超出FDA标准范围的崩解测试方法的可行性
Lukas Uebbing, Lukas Klumpp, Gregory K Webster, Raimar Löbenberg. Drug Design, Development and Therapy. April 2017.IF=3.216
16. 采用DDDPlus™模拟药物的体外溶出行为
Simulation of In Vitro Dissolution Behavior Using DDDPlus™
Almukainzi M, Okumu A, Wei H, Löbenberg R. AAPS PharmSciTech.Feb, 2015. IF=2.401
17. 体外-体内相关性IVIVC:通用概念,方法,在法规监管中的应用
In vitro–in vivo correlations: general concepts, methodologies and regulatory applications [J].
González-García I, Mangas-Sanjuán V, Merino-Sanjuán M, et al. Drug development and industrial pharmacy, 2015, 41(12): 1935-1947. IF=2.365
18. 生物相关性溶出度方法研究进展
缪慧,阮昊,陈悦,洪利娅. 《中国现代应用药学》. 2018,35(01). 综合影响因子:1.2
本文汇总了体外崩解与溶出模拟软件DDDPlus的应用案例及操作视频,如需观看,请点击下方链接查看。
请回到该产品介绍顶部,查看产品概述、模块简介、资料文献、应用案例


