【案例分析】以mTOR为靶点的抗EV71化合物的设计、合成及生物活性评价

导 读
本文针对目前临床上尚无有效药物的病毒性传染病,为如何快速开发广谱且不耐药的新化合物提供了指导。
参考文献作者及单位
Tianlong Hao, Yuexiang Li, Shiyong Fan, Wei Li, Shixu Wang, Song Li, Ruiyuan Cao,Wu Zhong
军事医学研究院国家应急防控药物工程技术研究中心
参考文献
1. 以mTOR为靶点的抗EV71化合物的设计、合成及生物活性评价
Design, synthesis and pharmacological evaluation of a novel mTOR-targeted anti-EV71 agent. Hao T, Li Y, Fan S, Li W, Wang S, Li S, Cao R, Zhong W. Eur J Med Chem. Apr 24, 2019. IF=4.833
2. 以mTOR为靶点的抗EV71化合物的设计、合成及生物活性评价
郝天龙,军事科学院博士学位论文
案例摘要
目的:以哺乳动物雷帕霉素靶蛋白mTOR为作用靶点,开发全新广谱且不耐药的抗EV71药物。方法:通过分析Torin2和mTOR蛋白之间的相互作用,共设计和合成了三大类新化合物。
结果:经过细胞水平,酶水平、分子水平的生物活性评价,优选体外活性较好5个化合物开展小鼠的药代动力学研究。
结论:根据体外活性、体内药代动力学、在水中溶解度等指标,最终有2个化合物可能是抗EV71治疗的潜在候选化合物。
软件用途
通过ADMET Predictor软件预测了化合物的吸收性质。凡默谷技术部建议还可在设计化合物时,进行化合物的ADMET性质预测,从而筛选出成药性更佳的化合物进行化学合成。
1. 研究背景
手足口病(Hand,Foot and Mouth Disease,HFMD)是一种严重威胁人类特别是儿童生命健康的传染病。根据国家卫生健康委员会报告,截至2015年,我国手足口病累计发病1176万余例,其中死亡3361例,居丙类传染病报告发病数榜首。
引发手足口病的主要病原体为肠道病毒71型(Enterovirus 71,EV71), 它具有高度传染性和变异性。目前临床上尚无有效抑制EV71的抗病毒药物,多数还处于研发阶段,因此研发高效抗EV71的药物日益迫切。
当EV71病毒侵染宿主细胞后,会触发细胞内PI3K/Akt/mTOR信号通路,进而激活哺乳动物雷帕霉素靶蛋白mTOR,为病毒的RNA复制和蛋白质合成提供物质基础。如有化合物能抑制宿主细胞mTOR蛋白,则可以阻止病毒RNA复制和蛋白质合成,从而抑制病毒感染。
通过对现有mTOR抑制剂的调研,发现Torin2是一种活性较好的mTOR抑制剂(IC50=0.25nM),本研究以Torin2作为先导化合物,对其进行结构优化,以期获得活性和成药性都良好的全新结构mTOR抑制剂。
2. 结果与分析
2.1 化学合成
通过分析Torin2和mTOR蛋白之间的相互作用,作者共设计了三大类新化合物,经过计算机虚拟筛选与合成可行性分析后,最终完成了98个新化合物的合成工作,且结构全部经MA,1HNMR进行确认。
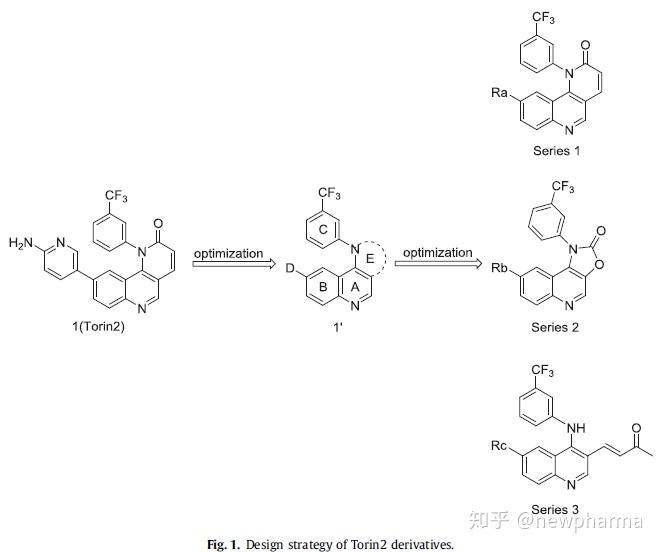
2.2 生物活性评价
该研究从细胞水平,酶水平、分子水平对所合成的化合物进行生物活性评价,分别评价了其对RD细胞系肠道病毒71型(EV71)H株的抑制活性、mTOR激酶抑制活性、mTORC1/ mTORC2抑制活性。
2.3 吸收与药代动力学评价
2.3.1 预测吸收性质
对活性较好的5个化合物进行了吸收性质的预测,ADMET Predictor软件的预测结果表明化合物11a, 11b, 11d, 11e, 11m的吸收风险系数Absn_Risk均小于3(风险阈值≤3,说明化合物的吸收较好)。
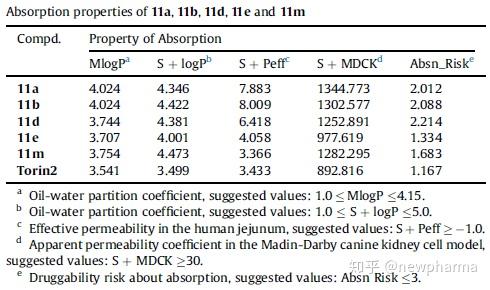
案例分析人建议:药物设计与结构优化阶段,可通过ADME/Tox预测软件评估所设计化合物的吸收、代谢、分布、排泄及毒性,从而快速淘汰药物代谢性质不佳或有潜在毒性的化合物。我们通过ADMET Predictor软件预测文中的16个的化合物11a-11o,预测结果中有5个化合物的综合风险系数ADMET_Risk大于7,分别是11i,11j,11m,11n,11o,且11m,11n,11o显示有潜在的hERG心脏毒性,建议不合成11m,11n,11o,而在早期设计出更多ADMET性质较佳的新化合物。
其中,整体风险系数ADMET_Risk综合吸收Risk,代谢Risk和毒性Risk的打分规则,对化合物进行全面的ADMET性质打分和成药性评估:对于大部分的药物分子,ADMET_Risk 打分值小于或等于7。
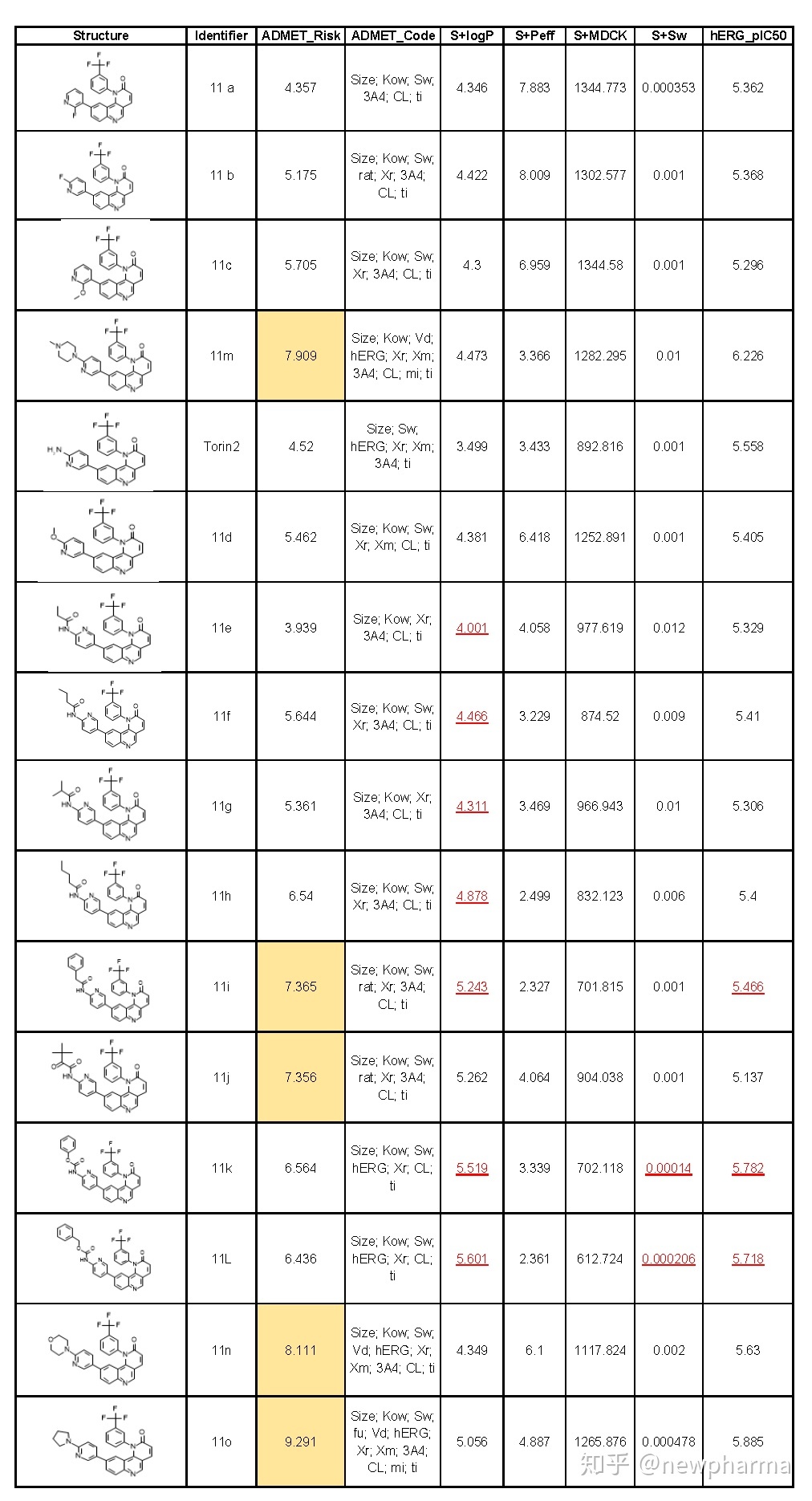
表1:采用ADMET Predictor预测化合物的ADMET性质
红色表示预测结果超出训练集范围,结果可信度不高
2.3.2 溶解度测试
因为大部分抗病毒药物为难溶性药物,即BCS II或IV类化合物,为后期的制剂研发带来了挑战,本研究还测试了体外活性较好的5个化合物在水中的溶解度,范围在0.4-19μg /ml。
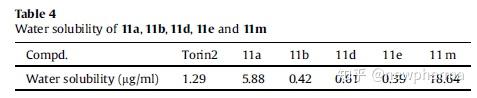
案例分析人采用ADMET Predictor预测了这五个化合物和先导化合物Torin2在水中的溶解度,预测结果为Torin2=1μg/ml,5个化合物的水溶性范围在0.4-12μg/ml,与试验结果(0.4-19μg /ml)基本吻合。此外ADMET Predictor还可预测化合物在胃肠道液中的溶解度,分别是:空腹下的胃液S+FaSSGF, 空腹下的肠液S+FaSSIF,餐后状态下的肠液S+FeSSIF。
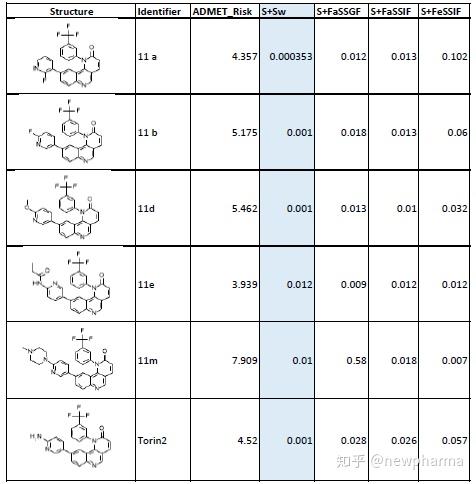
表2:采用ADMET Predictor预测化合物的在水中和胃肠道中的溶解度
溶解度的单位是mg/ml
2.3.3 体内药代动力学研究
此外,体外活性较好的5个化合物还开展了小鼠的体内药代动力学研究。分别是HTL-6-45=11e, HTL-6-48=11a, HTL-7-01=11b, HTL-7-03=11d, HTL-7-17=11m。其中HTL-6-48(11a),HTL-7-03(11d)和HTL-7-17(11m)的生物利用度均大于20%, 为有潜力的候选化合物。

3. 总结
本研究针对mTOR激酶,选择Torin2作为先导化合物进行优化设计,共设计和合成出喹啉类,五元环类和Torin2的抗EV71病毒化合物。对已合成的化合物进行体外抗病毒活性测试,结果显示Torin2类衍生物具有较高的体外抑制活性,部分化合物与先导化合物Torin2体外活性相当。通过分子机制研究,Torin2类衍生物属于mTORC1/ mTORC2的双重抑制剂。
接着,作者优选了5个活性优良的化合物开展了水溶性测试和动物的体内PK试验,并进行了初步的构效关系分析,为基于mTOR靶标的新型抗EV71抑制剂的研究提供了基础和方向。


