【建模文章解读】采用生理药代动力学模型考察羟考酮的药物相互作用DDI

摘 要
羟考酮是阿片类镇痛药物,在体内会产生具有药理活性的代谢产物且具有较窄的治疗窗。CYP3A4和CYP2D6是羟考酮形成代谢产物的主要代谢酶,抑制或诱导这两种酶的活性,将显著改变羟考酮及其代谢产物在体内的暴露量。
目的:期望采用GastroPlus软件搭建和验证羟考酮(母药)、2个一级代谢产物(noroxycodone去甲羟考酮、oxymorphone羟氢吗啡酮)、1个二级代谢产物(noroxymorphone去甲羟氢吗啡酮)的PBPK模型。并进一步用该模型预测羟考酮联合CYP3A4抑制剂(酮康唑、伊曲康唑及代谢产物)、CYP2D6抑制剂(奎尼丁)、CYP3A4诱导剂(利福平)给药后的DDI。
方法:所建立的模型基于文献、内部实验以及计算机预测的数据,并用文献报道的单独给药的临床PK数据对模型进行验证和优化;模型进一步用于羟考酮联合给药后的DDI预测。
结果:与观测值相比,DDI模型预测的AUC误差分别为:羟考酮-1.5倍;去甲羟考酮-1.8倍;羟氢吗啡酮-1.3到4.5倍;去甲羟氢吗啡酮-1.4到4.5倍(案例解读者建议:可进行群体DDIs的评估,以分析群体变异对DDI结果的影响,并和不同临床的结果进行比较)。
结论:该工作说明PBPK模型可用于预测母药及多个代谢产物与调节剂perpetrator联合给药后的DDI;虽然和单独评估母药的DDI相比,预测代谢产物DDI的准确性较低;但该案例提供了一种方法,即可评估母药与多种代谢产物,与CYP3A4(伊曲康唑有多个代谢产物)和CYP2D6调节剂合并用药后的DDI风险。

原文献作者
Jaana Rytkönen, Veli-Pekka Ranta, Merja Kokki, Hannu Kokki, Heidi Hautajärvi, Valtteri Rinne, Aki T. Heikkinen
1 芬兰Admescope Ltd
2 东芬兰大学药学院(芬兰)
3 芬兰库奥皮奥大学附属医院,麻醉和重症监护中心
4 东芬兰大学医学院(芬兰)
参考文献
Jaana Rytkönen, Veli-Pekka Ranta, Merja Kokki, et al., Physiologically based pharmacokinetic modelling of oxycodone drug–drug interactions. Biopharm Drug Dispos. 2020; 41: 72-88. IF: 1.611
推荐理由
本案例搭建及验证了羟考酮、2个一级代谢产物(去甲羟考酮与羟氢吗啡酮)、1个二级代谢产物(去甲羟氢吗啡酮)的PBPK模型,是学习母药及其代谢产物PBPK建模的参考资料;基于建立的底物PBPK模型,进一步考察联合不同类型的调节剂(CYP3A4抑制剂、CYP3A4诱导剂、CYP2D6抑制剂)给药后的DDI预测,因此是基于PBPK建模评估DDI的学习资料;此外,还能了解如何评估羟考酮及其活性代谢产物(3个)与伊曲康唑及其活性代谢产物(3个)复杂联合用药后的DDI。
1. 研究背景
药物-药物相互作用(DDI, Drug-drug interactions)会引起不良事件或导致疗效降低,是药物治疗常见的问题之一, 我国每年药物所致严重不良反应约250 万例,药物导致的死亡约20 万例。
在药物发现和开发过程,预测和洞见在研新药IND临床用药时的潜在药物相互作用DDI非常重要,因为DDIs可能会导致严重不良反应或治疗效果的降低。近年来,采用基于生理的药代动力学PBPK建模以评估和预测DDIs的方法日趋成熟,提交到法规部门的PBPK模型(指导给药方案以避免DDIs)也日渐增多。
PBPK模型的优势是可以解释复杂DDI的情形,整合多种机理或化合物进行DDI的风险评估。此外,如代谢产物对DDIs也有贡献或者具有药理学活性,也常整合到PBPK模型中,以预测共同作用后DDIs的结果。此外,PBPK模型还可以考虑更多的因素对DDIs的贡献,比如疾病状态、年龄等。
羟考酮是阿片类受体激动剂,用于急慢性的镇痛。羟考酮主要经肝脏代谢清除,主要的代谢酶为CYP酶;主要的一级代谢产物去甲羟考酮经CYP3A4代谢产生,另一个一级代谢产物(羟氢吗啡酮)则经CYP2D6作用产生,其它亚型酶的贡献可以忽略不计。
二级代谢产物(去甲羟氢吗啡酮)主要是去甲羟考酮被CYP2D6代谢产生,而羟氢吗啡酮到去甲羟氢吗啡酮的转化可以忽略不计。由于羟考酮及其代谢产物主要经CYP3A4和CYP2D6代谢清除,因此推测羟考酮和这些酶的调节剂联合服用后会产生较为明显的DDIs。而文献也有报道羟考酮联合用药,发现其体内暴露会升高2倍以上或下降50%,这将分别增强或减弱其药理活性。羟考酮的三个主要代谢产物都具有药理活性,目前通常认为该药物的活性主要来自羟考酮的药理活性,不过也有报道给药后可以达到羟氢吗啡酮的药理学相对浓度。
本案例的目的是期望采用GastroPlus软件建立和验证可预测羟考酮及其两个一级代谢产物、一个二级代谢的血药浓度-时间曲线的PBPK模型。并进一步用该模型预测羟考酮联合CYP3A4抑制剂(酮康唑、伊曲康唑)、CYP2D6抑制剂(奎尼丁)、CYP3A4诱导剂(利福平)给药后的DDI。
2. 建模数据与处理
2.1 羟考酮PBPK及DDI建模的相关参数
表1 羟考酮及其三个代谢产物的药物相关性质参数
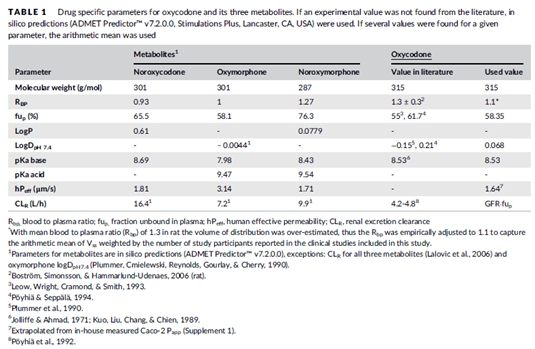
表2 PBPK模型中羟考酮及其代谢产物的主要代谢参数
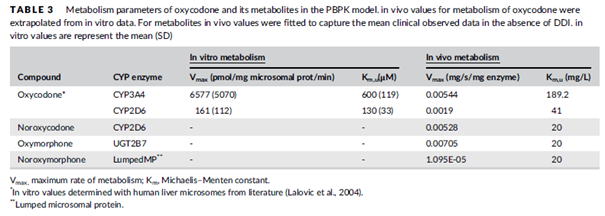
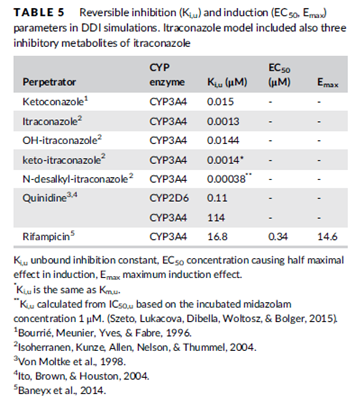
表3 DDI模拟中调节剂的抑制或诱导参数
2.2 数据获取及处理
2.2.1 基本建模参数的处理
输入到羟考酮PBPK模型的参数主要来自文献、及内部开展的体外数据(补充了Caco-2渗透性实验测定羟考酮的表观渗透性,以支持描述其胃肠道吸收特征)。如果文献中未报到相关的实验数据,还采用ADMET Predictor软件基于药物的结构式预测得到;如果可以找到某个参数的多个报道数值,则将算术平均值输入到模型中。羟考酮体内代谢的参数(Km, Vmax)通过体外数据转化而来,而代谢产物的体内数据则通过匹配临床平均PK数据优化得到。调节剂的抑制常数和诱导常数来自文献,伊曲康唑的三个代谢产物对CYP3A4的抑制特性也纳入到DDI模型中。模型的预测能力,通过文献报道的临床数据进行优化和验证。总共选择了17个临床研究(包括9个静脉给药、11个口服给药)的PK结果,以对比预测和观测的PK参数(如AUC, Vss, CL, Cmax, Tmax, F)、PK曲线的一致性。
2.2.2 口服吸收的预测
羟考酮的吸收过程采用GastroPlus内建的高级房室吸收与转运(ACAT)模型进行预测。文献报道羟考酮的溶解度在pH小于9.5时大于0.5 mg/mL,且溶解度对模型的预测能力也不敏感,因此不需进一步考察溶解度输入数值的准确性。
假设药物颗粒的粒径为25 μm并基于Johnson模型预测羟考酮的体内溶出行为;由于在溶液剂和胶囊剂中,未发现药物生物利用度和吸收速率的差异,预期溶出速率不是影响羟考酮吸收的限速步骤,因此未详细评估药物溶出速率的预测准确性。假设羟考酮经被动跨细胞扩散的方式通过胃肠壁,通过体外Caco-2细胞实验测定药物的表观渗透性并转为空肠的有效渗透性;采用Opt logD Model SA/V 6.1模型计算各个肠段的有效渗透性,该模型会考虑各个肠段pH、吸收面积的变化等。胃肠道模型选择ACAT默认的人体空腹状态,相关生理学参数未做调整,胃转运时间设定为0.25 h。
2.2.3 组织分布的计算
羟考酮的组织分布假设为血流限速型,并认为各个组织都为充分搅拌模型。设置为血流限速型组织是经过充分考虑的,主要为这种类型可以很好地吻合羟考酮血浆浓度-时间曲线,此外无论体内吸收还是体外Caco-2渗透性数据都表明羟考酮不是渗透性限速的药物。去甲羟考酮、羟氢吗啡酮、去甲羟氢吗啡酮也同样设为血流限速型组织分布,并认为是充分搅拌模型。虽然此前有报道羟考酮是以主动摄取转运的方式通过血脑屏障,提示其可能为P-gp的底物;但由于临床PK并没有明显的主动转运现象,且采用假设的血流限速型组织可以很好地表征羟考酮血浆PK行为,因此当前模型忽略主动转运对羟考酮血浆PK的贡献。采用GastroPlus内建的Lukacova公式计算组织分配系数(Kp),每一个模拟对象的生理学数据都采用内建的年龄相关的群体估算功能(PEAR)自动产生。组织游离分数(fu,t)采用GastroPlus默认的公式进行计算,该模型公式认为细胞外和细胞内空间非离子型游离浓度处于平衡状态。
2.2.4 代谢和清除的过程
下图显示了羟考酮以及代谢产物的体内转化过程。羟考酮通过CYP2D6和CYP3A4代谢成羟氢吗啡酮和去甲羟考酮;去甲羟考酮又进一步经CYP2D6代谢成去甲羟氢吗啡酮,其中忽略不计羟氢吗啡酮代谢生成去甲羟氢吗啡酮。羟氢吗啡酮的代谢主要经UGT2B7介导,并以葡萄糖醛酸产物经尿液排泄。由于缺少去甲羟氢吗啡酮更为细致的代谢数据,因此假设其通过肝脏微粒体代谢清除。此外,这四个化合物均考虑了肾脏排泄的清除。
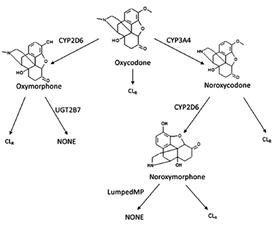
图1 PBPK模型中羟考酮及其代谢产物的清除机制
GastroPlus的人体生理学模型包含了CYP3A4, CYP2D6和UGT2B7在肠道及肝脏中的表达,此外UGT2B7还表达在肾脏中。基于假设每个组织具有相同的Vmax (per amount enzyme)和Km,u,并结合相应的酶分布水平,以计算这些酶在每个组织的具体Vmax。羟考酮的代谢数值是通过体外人微粒体的Vmax和Km,u数值进行转化得到的;对于羟考酮的代谢产物,设置了非饱和的Km数值(20 mg/L),Vmax数值则是通过匹配三组临床研究报道的代谢产物与母药AUC比例进行手动优化得到(该优化分为两步:首先是重现一级代谢产物的观测值;然后吻合二级代谢产物的结果)。
羟考酮的肾脏清除率(CLR)通过肾小球滤过率(GFR)*fup的方式计算得到;代谢产物的CLR则是来自口服15 mg羟考酮的临床尿排泄数据。
2.2.5 DDI模拟及调节剂模型的验证
验证后的羟考酮PBPK模型进一步开展DDI的研究:模型纳入了可逆CYP酶抑制剂-奎尼丁(CYP2D6),酮康唑(CYP3A4)和伊曲康唑 (CYP3A4)以及一个CYP3A4诱导剂-利福平;同时追踪羟考酮的代谢产物,以考察这些调节剂的影响。DDI模拟的方案设计如下表:
表4 DDI模拟的方案设计
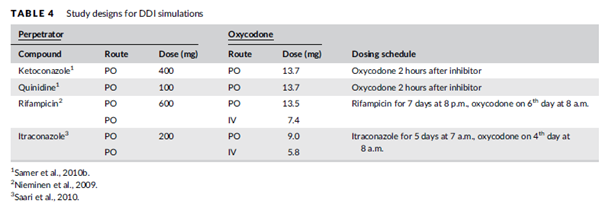
胃肠道模型基本设置为空腹状态(伊曲康唑的部分模型为餐后状态)。为了评估肠道代谢对DDI结果的贡献,分别考察了酮康唑和利福平对存在或没有肠壁代谢的羟考酮的DDI作用。采用蒙特卡洛模拟分析了CYP3A和CYP2D6的肝脏代谢贡献对羟考酮与酮康唑或奎尼丁DDI结果的敏感性:虚拟了30个个体,其肝脏CYP3A4和CYP2D6分布的CV介于119%和61%之间,并保持其它参数固定不变;不过这两个参数更多表征群体的变异,并未考虑CYP2D6的基因多态性。
对GastroPlus内建的酮康唑、奎尼丁、利福平模型不做任何调整,并用在羟考酮临床DDI试验中相同剂量水平的PK数据验证了这些调节剂的预测能力。模型预测的AUC、Cmax和t1/2等PK参数,与文献分别报道的酮康唑、奎尼丁、利福平临床结果较为接近,表明这些药物的内置模型具有较准确的预测性。对内建的伊曲康唑模型优化了沉淀模型,以匹配临床报道的伊曲康唑暴露:假设为非机制性的一级沉淀模型,并优化了伊曲康唑的沉淀时间。
3. 模型结果与分析
3.1 羟考酮及其代谢产物PBPK的搭建与验证
下图模拟的结果表明,预测与观测的AUCs,血浆中羟考酮的浓度曲线都在观测值的标准误差范围内;不过羟考酮的代谢产物预测结果与观测血药浓度-时间曲线相比要误差稍大一些。静脉给药后预测羟考酮的AUC在观测值的1.6倍误差内;所预测的羟考酮Vss和CL范围分别为174–285 L和29–66 L/h,而临床观测结果的范围分别为135–307 L和30–44 L/h。口服给药后预测羟考酮的AUC和Cmax相对观测值的误差分别为1.5和1.4倍;预测口服生物利用度的范围为39–48%,观测结果为55–69%;预测代谢产物的AUC及78%的Cmax相对静脉给药后观测结果的误差在2倍以内;口服给药后,86%的AUC和90%的Cmax在观测值的2倍误差范围内。
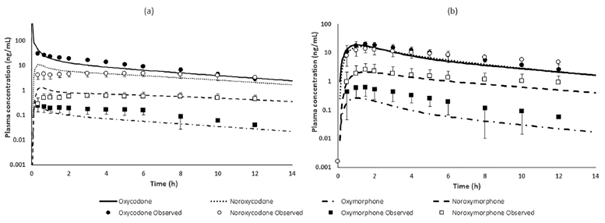
图2 静脉(a)及口服(b)给药后,羟考酮及其代谢产物的观测与预测血药浓度-时间曲线
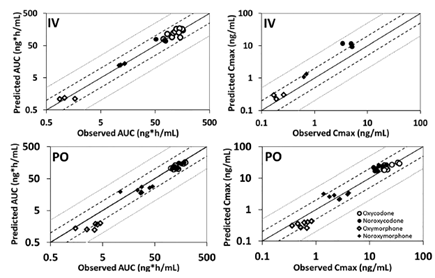
图3 静脉及口服给药后,羟考酮及其代谢产物观测与预测的AUC与Cmax (黑色及灰色虚线分别代表2倍与5倍的误差线,黑色实线代表完全一致的情况)
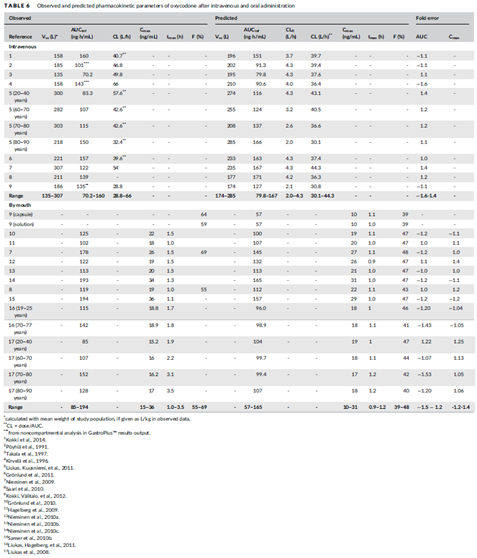
表5 静脉及口服给药后,羟考酮观测与预测的PK参数
3.2 优化伊曲康唑的模型
优化伊曲康唑的PK模型并使其没有沉淀的现象(沉淀时间设定为1 000 000 s),模拟结果见下图。与观测结果相比,预测伊曲康唑AUC和Ctrough的误差分别为1.7和1.5倍。
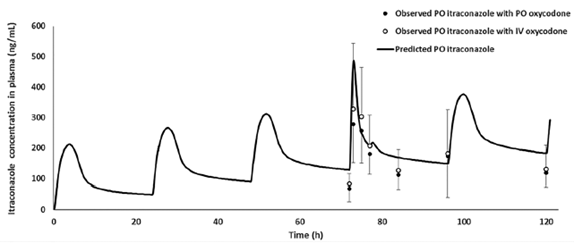
图4 口服200 mg伊曲康唑联合口服或静脉给药羟考酮后的观测与预测的血药浓度-时间曲线(观测结果来自临床试验的报道,伊曲康唑78小时处峰浓度的改变是因为胃肠道生理由空腹变为了餐后)
3.3 DDI模拟
下图为羟考酮与酮康唑、伊曲康唑、奎尼丁及利福平联合给药后的DDI模拟结果,提示采用羟考酮PBPK模型能很好地预测其AUCs的变化;代谢产物预测的PK曲线与观测数值也基本在一条直线上。所有预测的羟考酮以及去甲羟考酮AUCR和CmaxR都在观测结果的2倍误差范围内;对于羟氢吗啡酮和去甲羟氢吗啡酮,AUCR的2倍误差比例分别为83%和50%,CmaxR的2倍误差比例分别为83%和33%;除了利福平与静脉注射羟考酮的DDI预测外(羟氢吗啡酮的AUCR为4.5倍),所有调节剂对羟氢吗啡酮暴露影响(AUCR和CmaxR)的预测结果都在2倍误差范围内;去甲羟氢吗啡酮AUCR的预测误差范围为−1.09 – 4.5。
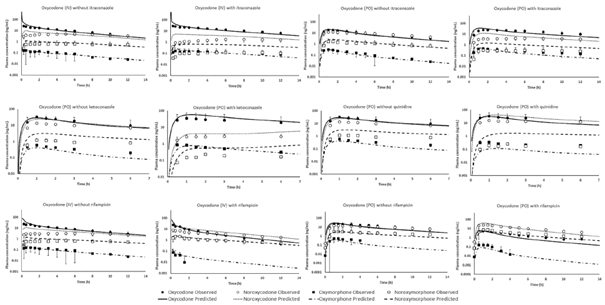
图5 羟考酮联合或无调节剂给药后,观测与预测的羟考酮及其代谢产物血药浓度-时间曲线
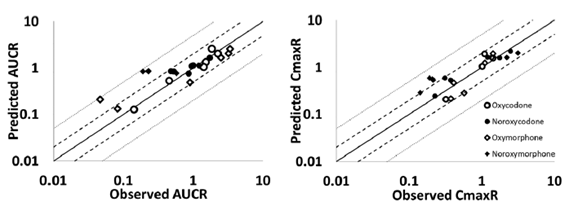
图6 DDI模拟中观测与预测的AUCR和Cmax R (黑色及灰色虚线分别代表2倍与5倍的误差线,黑色实线代表完全一致的情况)
表6 DDI模拟中预测与观测AUCR和CmaxR的误差
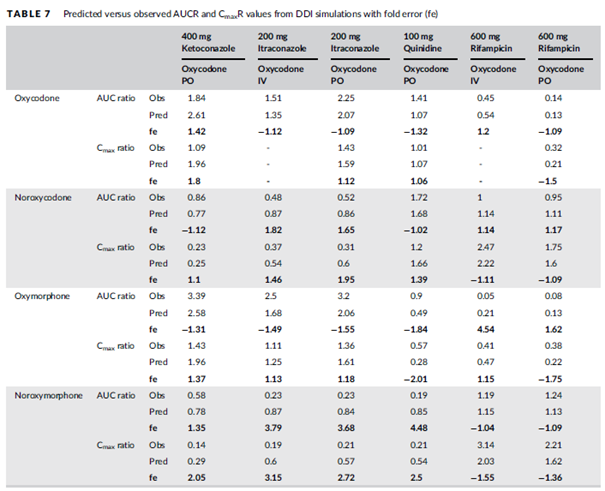
模型还进一步探索了有无肠壁代谢时对预测口服羟考酮DDI的影响:羟考酮和酮康唑联合给药后,存在或没有肠壁代谢时,预测的F%分别为81%和78%;预测的羟考酮CmaxR分别为1.96和1.59倍;AUCR分别为2.6和2.0倍。在联合利福平给药后,预测的F%分别为11%和22%;预测的羟考酮CmaxR分别为0.21和0.31倍;AUCR分别为0.13和0.21倍。
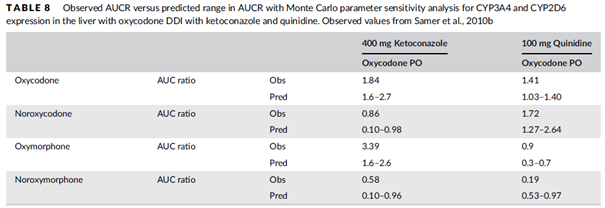
采用蒙特卡洛模拟分析了肝脏中CYP3A和CYP2D6的分布对羟考酮与酮康唑或奎尼丁DDI结果的敏感性:羟考酮联合酮康唑、奎尼丁给药后,预测的羟考酮、去甲羟考酮和去甲羟氢吗啡酮AUCR范围均涵盖了观测AUCR;羟氢吗啡酮平均观测AUCR稍超出预测范围,结果见下表:
表7 蒙特卡洛模拟分析肝脏中CYP3A和CYP2D6的分布对羟考酮与酮康唑或奎尼丁DDI结果的敏感性
4. 模型讨论
该研究搭建和验证了羟考酮及其三个主要代谢产物(去甲羟考酮、羟氢吗啡酮、去甲羟氢吗啡酮)的PBPK模型:和临床观测数据相比,静脉或口服给药后(无DDI时)预测羟考酮及其代谢产物暴露大部分(90%的AUC和Cmax)都在2倍误差范围内。模型进一步用于评估了羟考酮联合CYP2D6可逆抑制剂-奎尼丁、CYP3A4抑制剂-酮康唑和伊曲康唑、CYP3A4诱导剂-利福平给药后的DDI:模型预测羟考酮以及其代谢产物的83% AUCR和77% CmaxR都在观测结果的2倍误差范围内,说明假设的羟考酮到其代谢产物的路径以及所用的模型参数都较为合理;还进一步选择酮康唑和利福平,考察了有无肠壁代谢对预测口服羟考酮DDI的影响,表明羟考酮的肠壁代谢对其DDI的影响较弱。
结果提示相比单独评估母药的DDI,加入追踪代谢产物后预测结果具有较大的不确定性:这可能是因为母药到一级代谢产物、以及一级产物到二级代谢产物追踪的不确定与不准确性;此外当前模型没有纳入形成代谢产物的其它消除途径,这也可能使得代谢产物的预测结果有一定不确定性。当然由于CYP2D6基因多态性的影响,也使得临床代谢产物的观测结果具有较大的个体内、个体间变异。通过群体DDI的模拟,可以考察模型参数在一定范围内变化时的群体PK变异;此外,敏感性分析结果也说明肝脏CYP3A4和CYP2D6丰度会敏感影响羟考酮DDI的结果。
此外,准确的DDI参数和良好的调节剂的模型对于获得更准确的DDI结果也至关重要。该工作收集了文献报道的DDI参数,并对不同来源的数据进行了准确性比较;当前模型仅考虑了CYP酶介导的DDIs,忽略了UGT2B7的作用(因为在临床浓度下,UGT2B7相比CYP的作用较弱)。虽然可直接使用软件内建的调节剂模型,甚至软件开发者还验证了这些模型,但是使用者还是有必要确保在特定预测条件下模型具有较合适的表现。由于DDI模型中使用了预测的代谢位点处游离的调节剂浓度(实际中较难测定),因此该工作采用了文献报道的相同剂量水平下,对模型内建的调节剂(奎尼丁、酮康唑、利福平)的血浆AUC、Cmax、半衰期等PK参数与观测值进行了准确性比较。优化了伊曲康唑的模型(延长沉淀时间,假设体内不产生沉淀),因为内建模型不能与羟考酮DDI试验中报道的结果相吻合。为了评估伊曲康唑的代谢产物对DDI模拟结果的贡献,模型还评估了纳入三个代谢产物以仅使用一级代谢产物的预测表现:结果显示包含三个代谢产物的模拟结果,对预测羟考酮与伊曲康唑的DDI更准确。
FDA和EMA目前都鼓励申办方使用PBPK模型,评估新化合物的代谢产物对DDIs的贡献。当越来越多的应用案例进行报道,以及在不同平台测试DDI的预测结果,这种纳入代谢产物的PBPK建模以预测DDI的预测信心才会逐渐加强。虽然之前有报道采用SimCYP软件搭建羟考酮(包含两个一级代谢产物:去甲羟考酮和羟氢吗啡酮)PBPK模型,但当前采用GastroPlus软件还可以进一步建立二级代谢产物(去甲羟氢吗啡酮)的PBPK模型。羟考酮和伊曲康唑的模型非常有效地展示了PBPK模型对包含复杂行为的DDIs预测能力,因为该模型包含了两个母药,同时还纳入了6个代谢产物。由于代谢产物形成及处置具有较复杂的途径,这使得整合代谢产物到PBPK模型具有一定的挑战性,但PBPK模型依然被认为研究和理解预测整合代谢产物的DDIs的一种有用工具。
5. 总结
该工作采用GastroPlus软件搭建了羟考酮及其主要代谢产物(去甲羟考酮、羟氢吗啡酮、去甲羟氢吗啡酮)的PBPK模型,可很好地重合文献报道的静脉或口服给药后的PK数据;接着,模型进一步用于评估羟考酮与CYP2D6可逆抑制剂-奎尼丁、CYP3A4抑制剂-酮康唑和伊曲康唑、CYP3A4诱导剂-利福平联合给药后的DDI情况。
该工作展示了如何搭建母药及代谢产物追踪的PBPK模型(特别是形成代谢产物的体外数据不齐全的情况),此外还展现了PBPK模型对底物与调节剂(可以包含一系列代谢产物)联合给药后DDIs的预测能力。所建立的羟考酮及其代谢产物的PBPK模型还可进一步用于预测其他人群(如儿童、器官损伤等)的临床PK以及DDIs (与其它CYP2D6和CYP3A4的调节剂联合给药)。
但模型包含代谢产物后,与单独母药的DDIs预测结果相比,其模型的复杂程度升高了,其预测结果的准确性降低了,因此在这解释与使用这种复杂模型的DDI预测结果时,需综合衡量利弊。
6. 应用软件与模块
该案例应用的软件是GastroPlus (version 9.5.0004),涉及模块有Base, PBPK, PKPlus, Metabolism & Transporter, DDI;ADMET Predictor (version 7.2.0.0),涉及模块有PhysChem, Metabolism。


