【建模文章解读】比较传统反卷积与吸收机制建立的IVIVC模型在BCS III类候选药物缓控释制剂处方开发中的应用
导读
为促进制药同行对建模与模拟方法的深入理解,多参考国内外同行建模的思路与流程,深入理解应用案例中建模的要点;凡默谷技术部精心挑选了建模与模拟较有特色的文章进行剖析解读,希望对您有帮助。
解读人:凡默谷王钰玺
推荐理由
默沙东美国研发中心比较了传统反卷积与吸收机制建立的IVIVC模型在BCS III类候选药物缓控释制剂处方开发中的应用。通过优化胃肠道模型中的吸收放大因子(ASF)建立了机制性反卷积的IVIVC模型,该模型对不同释放速率制剂的Cmax和AUC均可进行准确的预测,相比传统反卷积建立的IVIVC模型平均预测误差更小,对该药物后续处方的开发具有重要的指导意义。此外,这种通过调整模型参数建立IVIVC的方法,为IVIVC模型的建立提供了一种新思路。
文献摘要
默沙东以MK-0941为模型药物,建立并比较传统反卷积与基于吸收机制的IVIVC模型中的特点。采用两类制剂(骨架片和多粒小丸胶囊)、每类制剂又分别3种不同释放速率的处方建立IVIVC模型。传统反卷积和机制性IVIVC这两种模型与两类制剂的AUC和Cmax的平均预测误差分别低于10%和15%。
这两种A级相关的IVIVC模型均可用于表征MK-0941的药动学参数并为后续的处方开发提供指导,基于吸收机制性的IVIVC模型拓展了传统IVIVC在缓控释制剂处方开发中的应用。
1. 研究背景
IVIVC是一种可预测性模型,用于表征某特定药物溶出和血药浓度之间的关系。建立IVIVC模型对指导制剂处方的开发起着越来越重要的作用,特别是对缓控释制剂,其处方组成对药物进入体循环的影响更为显著。
监管机构(如FDA)也出台了不同IVIVC水平的指导文件。建立IVIVC的方法通常采用反卷积法,近几年来随着基于吸收机制性的PBPK模型的发展为处方和PK的连接提供了新思路,该模型涉及口服吸收的关键过程,包括药物的溶出、肠道渗透等,再结合药物的清除及分布参数预测药物的药时曲线。基于吸收机制的PBPK模型建立相关性比传统的反卷积法需要输入更多的胃肠道生理参数,同时也有更灵活的适用性。
本案例以BCS III类候选药物MK-0941为模型药物,分别基于传统的反卷积法和基于吸收机制的PBPK模型建立了IVIVC,并用临床实测数据进行了验证。
2 建模数据与处理
2.1 MK-0941的相关建模参数
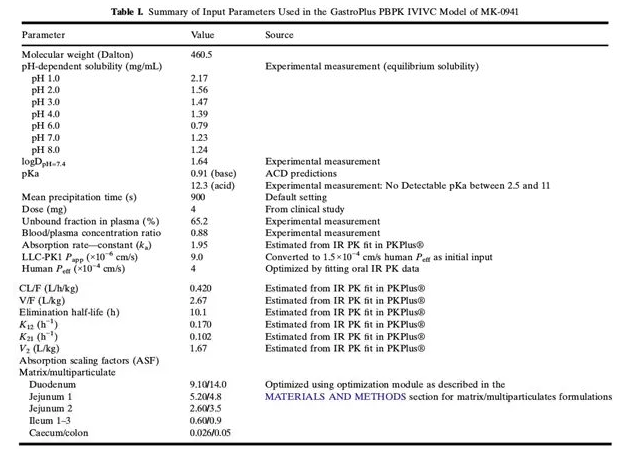
2.2 处方与溶出
制剂类型一:HPMC(羟丙基甲基纤维素)骨架片,通过调节HPMC的含量控制释放速率,共有三种释放速率的处方;制剂类型二:多粒小丸处方组成核心,乙基纤维素包衣,通过包衣的量控制药物的释放速率,也有三种释放速率的处方,且保持和骨架片同样的释放速率。下图T80 8h表示8小时释放80%;溶出方法:USP桨法100 rpm。
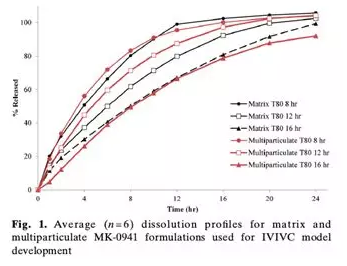
2.3 数据获取及处理
理化参数:不同pH下的溶解度、pKa、logP、血浆蛋白结合率、全血血浆浓度比均采用实测结果。
渗透性采用实测的LLC-PK1细胞的渗透性转化为人肠道渗透性,又通过口服速释制剂对该数值进行了优化,最终人肠道的Peff为4×10−4cm/s。由口服速释制剂的PK曲线通过PKPlus模块计算得到清除及分布参数。
临床试验数据:开展16例健康受试者以随机、交叉的的临床试验,治疗组包括安慰剂和4mg剂量的骨架片、多颗粒胶囊和速释胶囊。
临床PK试验结果:
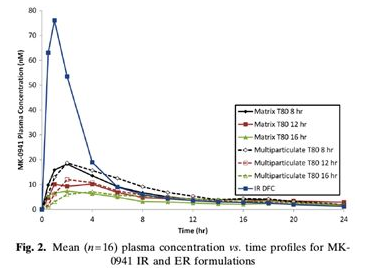
药动学参数汇总:
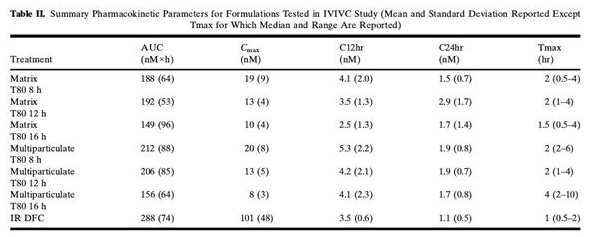
3 模型结果与分析
3.1 基于传统反卷积建立的IVIVC模型
建模要点:
建模要点:分别对两类制剂实测的PK曲线进行了反卷积,得到各处方的体内吸收曲线(Fig. 3),再分别结合体外溶出曲线建立IVIVC,得到两类制剂分别对应的平均体内外相关性(Table III)。分别用各制剂的体外溶出曲线,借助已建立的体内外相关性预测内体PK,并与实测结果进行比较(内部验证,Fig. 4, Table IV)。
两类制剂,六种处方反卷积后得到吸收-时间曲线:
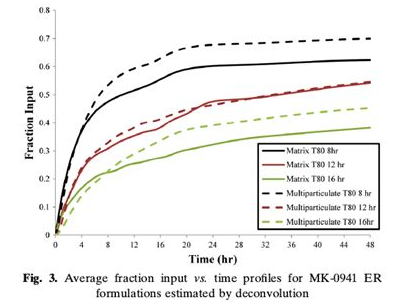
体内外相关性具体参数:
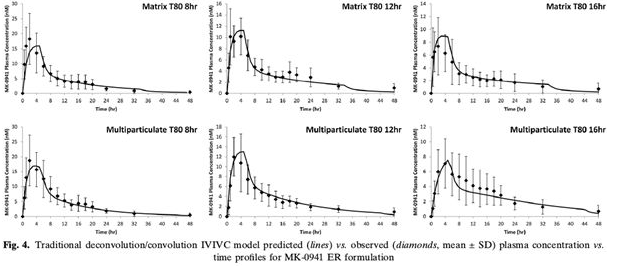
用传统反卷积建立的IVIVC模型的预测结果(线为预测结果,点为实测结果):
预测结果与实测结果的PK参数比较:
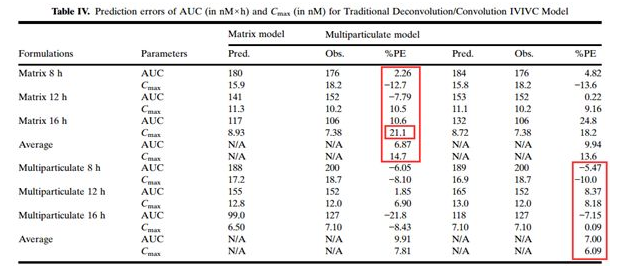
结果:基于传统的去卷积建立的IVIVC模型成功预测了MK-0941骨架片快速释放(T 8h)和中速释放(T 12h)处方的PK曲线(PE < 15%,Table IV),但慢速释放处方的预测结果偏高(PE > 15%);模型对不同释放速率的多颗粒小丸胶囊均实现准确的预测。
3.2 基于吸收机制的IVIVC模型
建模要点:
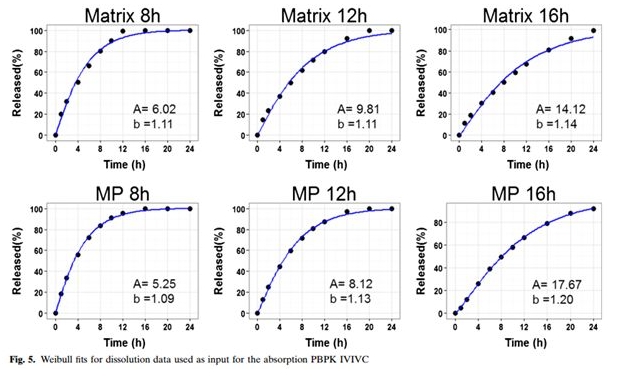
基于吸收机制的IVIVC模型胃肠道部分是基于GastroPlus 8.0的胃肠道高级房室吸收与转运模型(ACAT模型,该模型已内建了胃肠道的生理参数)的默认模型参数:Opt-logD model SA/V 6.1;结合PKPlus模块计算得到的清除及分布参数确定处置模型,使用Weibull方程拟合体外溶出曲线,并优化了吸收放大因子(ASF)。
Weibull方程拟合体外溶出的结果:
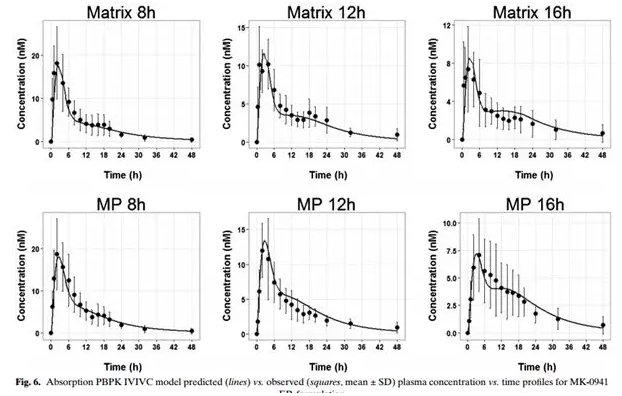
基于吸收机制建立的IVIVC模型的预测结果(线为预测结果,点为实测结果):
预测结果与实测结果PK参数的比较:
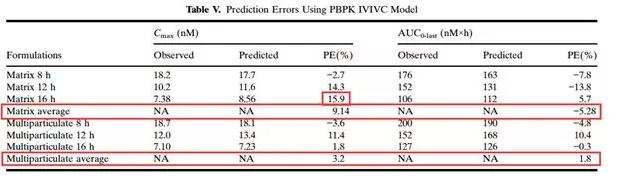
结果:
基于吸收机制的IVIVC模型,成功预测了MK-0941骨架片快速释放(T 8h)和中速释放(T 12h)处方的PK曲线(PE < 15%,Table IV),但慢速释放处方的Cmax预测结果略微偏高(PE=15.9% > 15%)。对不同释放速率的多颗粒小丸胶囊的Cmax和AUC均实现了准确的预测,且平均预测误差较小,分别为PE(%)Cmax =3.2, PE(%)AUC=1.9。
4 模型讨论
基于传统反卷积法是建立缓控释制剂IVIVC模型的常用方法,但传统反卷积法仅适用于化合物的药代动力学参数完全是线性的情况;本案例中总的体内吸收表现出体外释放速率的依赖性(不同释放速率的处方生物利用度不同),因此建立线性模型比较困难。通过结合研究报道的肠段吸收依赖性、分段吸收的药物模型,采用分段的线性吸收比例,优化后的模型显著提升了体内外相关性,提高了预测准确性。虽然该IVIVC模型没有完全达到监管部门的标准(基质片慢速释放处方Cmax预测结果偏高),但当前的IVIVC模型对于指导MK-0941的早期处方开发仍具有重要的意义。
基于吸收机制的IVIVC模型同样是参考文献报道的出现同样预测误差的药物模型,采用了相同的处理方式—优化ASF值(吸收放大因子)。优化后的模型对两类制剂六种处方的预测结果仅基质片慢速释放处方的预测出现偏差(PE=15.9% > 15%),其余5种处方均符合监管部门的内部验证标准。
通过比较采用传统反卷积建立缓控释制剂IVIVC模型与基于吸收机制的IVIVC模型,原文作者发现这两种模型预测结果相近,均可以较好地预测两类制剂六种处方的PK。传统反卷积的IVIVC模型需要采用分段的线性吸收比例来表述模型;而基于吸收机制的IVIVC模型需要调整胃肠道模型(ACAT模型)的ASF,实际上这两种做法是考虑药物存在不同肠段吸收速率差异的类似方法。
这两种模型的主要区别在于:传统IVIVC模型是建立了体外溶出和体内吸收之间的相关函数;基于吸收机制的IVIVC模型是假定体外溶出代表体内释放,通过调整ASF因子实现对药代动力学参数的准确预测,可以认为是把制剂的不同释放行为用生理参数形式的展示。
此外,还有其它方法建立基于吸收机制的IVIVC模型(本文作者使用Weibull方程拟合体外溶出,再基于Weibull方程预测体内PK。小编提示:由体内的PK曲线结合ACAT模型,通过Weibull方程反卷积得到体内吸收曲线,同样可以建立了体内吸收与体外溶出的相关性)。由于没有可以证明MK-0941存在肠段吸收差异的详细研究结果,无法进行单独拟合ASF值。对于缓控释制剂,ASF值与最终的体内外相关性相互影响,本文仅采用了较为简单的处理方式:即基于体外溶出预测体内PK的结果拟合ASF值。尽管本文没有提出更优的解决方案,但就MK-0941目前的模型预测结果而言,基于吸收机制的IVIVC模型可以作为传统IVIVC方法的替代方法,并用于指导早期MK-0941缓控释制剂的开发。
5 总结
在缓控释制剂处方开发过程中建立IVIVC很有必要,本研究表明对具有肠段吸收依赖性的BCS III化合物,传统反卷积的A级IVIVC和基于吸收机制的IVIVC均能准确反映化合物的药代动力学以指导制剂的开发。之前,关于吸收机制的IVIVC的文献报道较少,本案例突出了该方法的潜在效用,以拓展传统IVIVC方法在缓控释制剂处方开发中的应用。
6 应用软件与模块
该案例应用的软件是GastroPlus (version 8.0),涉及模块有Base, PKPlus, Optimization, IVIVC。
参考文献
Kesisoglou, F.; Xia, B.; Agrawal, N. G. Comparison of Deconvolution-Based and Absorption Modeling IVIVC for Extended Release Formulations of a BCS III Drug Development Candidate AAPS J. 2015, 17, 1492– 1500 IF: 3.423


